
11β-羟化酶缺乏症是什么?PGT-M能起到孕前干预的作用吗?

在医学的广阔领域中,总有一些疾病因其罕见性和复杂性而备受关注。11β-羟化酶缺乏症(11β-hydroxylase deficiency)便是其中之一。这是一种先天性肾上腺皮质增生症,其发病率虽然不高,但对患者的生活质量和健康状况有着深远的影响。今天橄榄树生命将为您详细介绍11β-羟化酶缺乏症,并探讨胚胎植入前遗传学检测(PGT-M)在孕前干预中的作用。

11β-羟化酶缺乏症是什么?
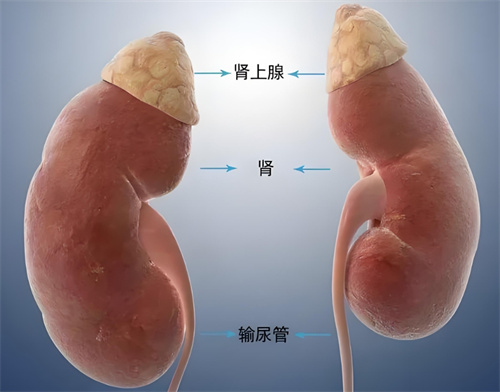
11β-羟化酶缺乏症于1955年首次被报道,是一种由于11β-羟化酶基因缺陷导致的遗传性疾病。该酶在肾上腺皮质中起着至关重要的作用,参与皮质醇和醛固酮的生物合成。当11β-羟化酶缺乏时,皮质醇的合成会减少,而11-去氧皮质醇和11-去氧皮质酮等前体类固醇会蓄积,导致雄激素过多。
该疾病的临床特征主要包括高血压、皮肤色素沉着、男性性早熟(在女性中表现为外生殖器男性化)以及高血钾和低血钠等症状。其中,高血压是最常见的表现,约见于2/3的患者,多为轻至中度高血压,由DOC分泌过多造成水、钠潴留和血容量扩张所致。
11β-羟化酶缺乏症为常染色体隐性遗传,这意味着患者需要从父母双方各继承一个缺陷基因才会发病。虽然该病的整体发病率较低,但在某些特定人群中,如中东的犹太人和阿拉伯人,发病率相对较高。
11β-羟化酶缺乏症的发病机理
酶特性:CYP11B1酶位于腺粒体内膜,负责催化11-去氧皮质醇和11-去氧皮质酮分别转变为皮质醇和皮质酮。当该酶缺陷时,皮质醇的合成减少,促肾上腺皮质激素的分泌增多,导致酶催化反应步骤的前体类固醇蓄积,进而引发疾病。
基因:CYP11B1基因定位于第8号染色体的长臂(8q),由9个外显子组成,在肾上腺皮质束状带表达,并受促肾上腺皮质激素的调节。11β-OHD是由CYP11B1基因突变所致,常见的突变形式包括无义突变、误义突变、变构突变和3个核苷酸插入,其中半数以上的突变发生在外显子6——8。无义突变通常导致较严重的临床症状,而不均一性突变的患者则症状较轻。
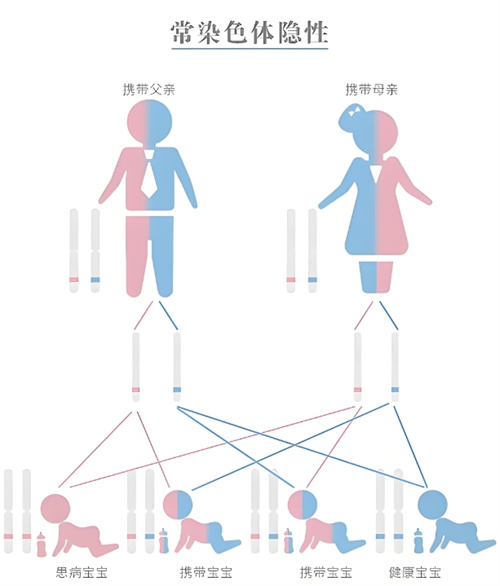
遗传特性:家系分析资料显示,11β-OHD为常染色体隐性遗传。这意味着患者必须从父母双方各继承一个致病基因才能发病。此外,CYP11B2酶基因亦定位于8q,与CYP11B1基因串连排列,且93%的氨基酸同源。但CYP11B2突变主要引起低血钠和高血钾,而不影响11-去氧皮质醇的11β-羟化作用,故不导致男性化。
11β-羟化酶缺乏症的临床表现
1.经典型
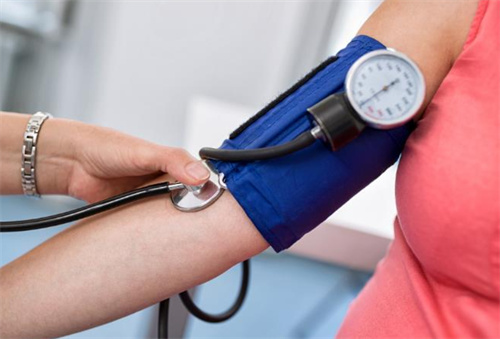
高血压是11β-羟化酶缺乏症显著的症状之一,约见于2/3的患者。患者的血压通常表现为轻至中度升高,这是由于11-去氧皮质酮分泌过多所致。11-去氧皮质酮的过量分泌会导致体内水、钠潴留,进而引发血容量扩张,导致血压升高。
同时,11β-羟化酶缺乏症患者皮肤上的色素沉着通常比CYP21缺乏症患者要轻一些。这种色素沉着与促肾上腺皮质激素水平的增高密切相关。促肾上腺皮质激素的升高会刺激肾上腺皮质分泌更多的激素,其中包括那些能够促进黑色素合成的激素,从而导致皮肤色素沉着。
患者的身体直线生长速度会加快,骨骺成熟速度也会提前,导致骨龄比实际年龄要大。这种生长加速的现象可能会对患者的身高和骨骼发育产生长期影响。
2.轻型
轻型11β-羟化酶缺乏症包括迟发型和隐型两种。这类患者的病情相对较轻,在出生时没有相关症状。然而,在青春期前后或成年期,患者可能会出现雄激素增多的症状,如多毛、痤疮等。值得注意的是,轻型患者通常不会出现高血压症状。

面对11β-羟化酶缺乏症这样的遗传性疾病,如何进行有效的孕前干预成为了医学界关注的焦点。幸运的是,随着辅助生殖技术和遗传学诊断的飞速发展,胚胎植入前遗传学检测(PGT)为我们提供了前所未有的可能性。
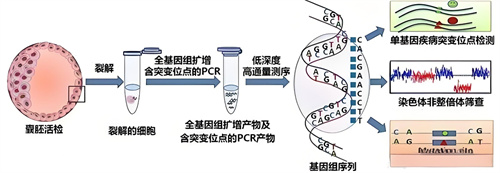
PGT-M,即胚胎植入前单基因遗传学检测,是一种针对单基因遗传病的孕前干预技术。它可以在胚胎植入子宫前,对胚胎进行遗传学诊断,筛选出携带致病基因的胚胎,从而避免遗传性疾病的传递。
对于11β-羟化酶缺乏症这样的常染色体隐性遗传病,PGT-M可以精准地检测出携带缺陷基因的胚胎,并筛选出健康的胚胎进行移植。这样一来,患者夫妇就有可能生育出健康的后代,避免遗传性疾病的再次发生。
11β-羟化酶缺乏症是一种罕见的遗传性疾病,对患者的健康和生活质量造成了严重的影响。然而,随着辅助生殖技术和遗传学诊断的不断发展,PGT-M技术为我们提供了孕前干预的新希望。通过精准地检测出携带致病基因的胚胎,并筛选出健康的胚胎进行移植,患者夫妇有可能生育出健康的后代,从而避免遗传性疾病的再次发生。虽然PGT-M技术还面临着一些挑战和局限性,但随着技术的不断进步和成本的逐渐降低,我们有理由相信,未来将有更多的遗传性疾病患者受益于这项技术。


顾问Chris